L’ibridazione sp3 e il legame semplice
L’atomo di carbonio, che allo stato eccitato possiede quattro elettroni di valenza, tornando allo stato fondamentale dispone i suoi quattro elettroni in altrettanti orbitali tutti uguali tra loro, fondendo in un unico strato quello s e quello p. I quattro orbitali così mescolati risultano ibridi, non appartenendo più né alla categoria s né alla categoria p e vengono perciò detti orbitali ibridi del tipo sp3, dove il numero esponenziale indica che sono tre gli orbitali p coinvolti nell’ibridazione.
Il carbonio ibridizzato sp3 è definito carbonio saturo. Esso può formare quattro legami covalenti di tipo σ con altri atomi di carbonio o di altri elementi, dando vita a geometrie tetraedriche in cui tutti i legami σ possono avere una libera rotazione.
I quattro orbitali ottenuti dall’ibridazione presentano per 1/4 le caratteristiche dell’orbitale 2s e per 3/4 le caratteristiche degli orbitali 2p e l’energia che possiede l’elettrone per rimanervi risulta leggermente inferiore a quella degli orbitali 2p e superiore a quella dell’orbitale 2s.
La forma che essi presentano è quella lobata, con due lobi di cui uno molto ridotto e uno di maggiori dimensioni.
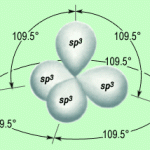
La geometria tetraedrica consente ai quattro orbitali ibridi di porsi alla massima distanza possibile rendendo minima la loro repulsione elettrostatica e corrisponde alla geometria prevista dalla teoria VSEPR.
Attraverso esperimenti chimici e misure spettroscopiche è stato dimostrato che la molecola del metano CH4, il composto organico più semplice, presenta una struttura tetraedrica regolare portante al centro l’atomo di carbonio e ai vertici quattro atomi di idrogeno a esso legati con angoli di 109,5°.
Questa struttura geometrica porta alla perfetta equivalenza dei quattro legami C—H, che è giustificabile solo se si ammette che i quattro orbitali del carbonio si mescolino tra loro per formare quattro nuovi orbitali ibridi tutti uguali, detti sp3.
La molecola del metano si forma grazie alla massima sovrapposizione dei quattro orbitali ibridi sp3 del carbonio con gli orbitali 1s dei quattro atomi di idrogeno dando vita a quattro legami semplici denominati legami σ (sigma).
Per la versatilità con cui gli orbitali sp3 sono in grado di congiungersi, questo tipo di ibridazione può dar vita a un numero considerevole di molecole contenenti da due a un numero infinito di atomi di carbonio.
Essi infatti possono accoppiarsi ad altri orbitali sp3 di altri atomi di carbonio dando vita così anche a legami C—C. Questo legame sarà senza dubbio covalente omopolare, in quanto la nuvola elettronica comune ai due atomi di carbonio è equamente distribuita.
E’ stato possibile misurare sia la lunghezza dei legami C—C sia quella dei legami C—H e sono rispettivamente 1,53 Å e 1,10 Å.
E’ stato possibile misurare sperimentalmente sia l’energia di legame C—C sia quella del legame C—H e sono rispettivamente 88 Kcal/ mol e 104 Kcal/mol.
I valori delle energie di legame permettono di rilevare che questi legami sono particolarmente forti.
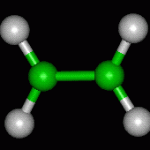
Le varie disposizioni che gli atomi assumono nello spazio per la rotazione dei gruppi intorno al legame σ sono dette conformazioni. La molecola dell’etano C2H6 presenta due conformazioni fondamentali denominate eclissata e sfalsata.
La conformazione eclissata è quella in cui gli atomi di idrogeno appartenenti a un atomo di carbonio ricoprono quelli appartenenti all’altro se la molecola viene osservata lungo la direzione del legame C—C.
La conformazione sfalsata è quella in cui gli atomi di idrogeno risultano perfettamente sfalsati se la molecola viene osservata allo stesso modo. Questa conformazione risulta più stabile di quella eclissata in quanto tutti gli atomi si trovano alla massima distanza l’uno dall’altro e perciò esercitano tra loro la minore repulsione.
Ogni atomo di carbonio può legarsi fino a un massimo di quattro atomi di carbonio dando vita così a catene lineari, ramificate o a strutture cicliche.



 Qualche decennio dopo, J. von Liebig analizzò accuratamente la composizione di un gran numero di sostanze organiche e fu capace di dimostrare che esse risultano dalla composizione di un numero limitato di elementi, ossia carbonio, idrogeno, ossigeno e azoto. L’analisi rivelò due fattori importanti:
Qualche decennio dopo, J. von Liebig analizzò accuratamente la composizione di un gran numero di sostanze organiche e fu capace di dimostrare che esse risultano dalla composizione di un numero limitato di elementi, ossia carbonio, idrogeno, ossigeno e azoto. L’analisi rivelò due fattori importanti: Kekulé e Couper riuscirono a spiegare la formazione di molecole organiche molto complesse applicando il concetto di valenza ai composti organici, già noto in chimica inorganica. Essi fornirono un metodo efficiente e semplice per rappresentare molecole molto organiche anche notevolmente complesse.
Kekulé e Couper riuscirono a spiegare la formazione di molecole organiche molto complesse applicando il concetto di valenza ai composti organici, già noto in chimica inorganica. Essi fornirono un metodo efficiente e semplice per rappresentare molecole molto organiche anche notevolmente complesse.